Справочник химика 21
Определение: Термодинамика - наука о закономерностях превращения энергии. Определение: термодинамической системой называется совокупность материальных тел, взаимодействующих, как между собой, так и с окружающей средой. Все тела находящиеся за пределами границ рассматриваемой системы называются окружающей средой. Поскольку одно и тоже тело, одно и тоже вещество при разных условиях может находиться в разных состояниях, пример: лед—вода—пар, одно вещество при разной температуре вводятся, для удобства, характеристики состояния вещества - так называемые параметры состояния. Температура тел - определяет направление возможного самопроизвольного перехода тепла между телами. В настоящее время в мире существует несколько температурных шкал и единиц измерения температуры..












В молекулярно-кинетической теории внутренняя энергия составляется из кинетической энергии всех частиц, потенциальной энергии взаимодействия молекул и энергии колебательного движения атомов т. Внутренняя энергия - функция состояния, зависящая от температуры и давления, а для идеального газа - только от температуры в этом случае потенциальной энергией взаимодействия пренебрегают. Таким образом, изменение внутренней энергии идеального газа равно произведению средней теплоемкости при постоянном объеме на разность температур газа. Энтальпия теплосодержание насыщенного газа — количество теплоты, необходимое для повышения температуры 1 кг вещества от абсолютного нуля до пара заданной температуры. В общем случае энтальпия является функцией температуры и давления.





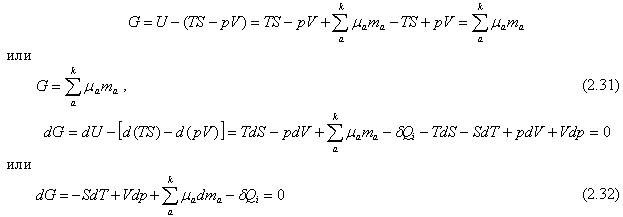
| 2 | Регистрация Вход. Ответы Mail. | |
| 467 | При решении задач Теормата Еремина в задачах часто жидкость испаряется, переходя в газ. | |
| 399 | Из уравнения для дифференциала внутренней энергии [9] [10] :. | |
| 491 | Вещества в химии. Химические реакции. | |
| 222 | Забыли пароль? Автор: Guzhelya , 2 Мая в Измерения. | |
| 202 | Многие термодинамические расчеты облегчаются при использовании аддитивных свойств термодинамических тел, называемых энергетическими или калорическими параметрами состояния функции состояния, получаемые расчетным путем. Такое название эти параметры состояния получили потому, что в их размерностях присутствует единица энергии [Дж] или [ккал]. | |
| 192 | Внутренняя энергия. | |
| 339 | Учебные материалы по физической химии Задачи по физической химии. | |
| 194 | Напишите мне в чат, пришлите ссылку на эту страницу в чат, оплатите и получите файл! Закажите у меня новую работу, просто написав мне в чат! | |
| 11 | Добрый день! |
Внутренняя энергия — функция состояния ТС, определяемая тем, что ее приращение в любом процессе, происходящем в закрытой системе, равно сумме теплоты, сообщенной системе, и работе, совершенной над ней. Всякая ТС имеет однозначную функцию состояния, называемую внутренней энергией, изменяющуюся только под влиянием внешних воздействий в процессе перехода системы из одного состояния в другое. В тех случаях, когда в некотором процессе изменения состояния закрытой ТС ее кинетическая и потенциальная составляющие энергии как единого тела, не изменяются, равенство принимает вид. Энтальпия — функция состояния ТС, равная сумме внутренней энергии и произведения объема на давление:.